近日,我校物理科学与技术学院计算物质科学团队孙运祥副教授及童朝晖教授携手Clemson大学丁锋教授,在纳米材料领域权威期刊《Small》(IF:15.153)上发表了题为“Molecular Insights into the Self-Assembly of Block Copolymer Suckerin Polypeptides into Nanoconfined β-Sheets”的学术论文,宁波大学为第一单位,孙运祥副教授和Clemson大学丁锋教授为共同通讯作者,2020级硕士研究生刘钰莹为论文第一作者。该研究得到国家自然科学基金(No. 11904189)的支持。
鱿鱼环齿(Suckerin)聚合物自组装材料所展现出的优异的热塑性、敏感的pH 响应性、良好的生物降解性和生物相容性,使其在药物输运、3D打印、人造组织等领域具有广泛的应用前景。Suckerin是由两种不同氨基酸序列模块交替排列形成的嵌段多肽共聚物:富含丙氨酸和组氨酸的M1模块和富含甘氨酸和酪氨酸的M2模块。揭示Suckerin的自组装机制,不仅有助于推动Suckerin嵌段多肽共聚物组装材料在纳米科技和生物医学中的应用,也会对未来新型仿生多肽纳米智能材料设计提供理论指导。
该研究利用快速离散分子动力学模拟方法,探究了Suckerin嵌段多肽的聚集动力学过程和相行为,揭示了Suckerin嵌段多肽共聚物的自组装分子机制。该研究发现:M1多肽模块β-sheet结构倾向性强但热稳定性差;M2多肽模块聚集倾向性强但结构有序度差;M1和M2聚集倾向的差异性使得Suckerin嵌段多肽产生“微相分离”组装复合结构体,聚集倾向性更强的M2模块会塌缩成柔软的“分子胶”,M1则被限制在M2分子胶簇的周围以β-sheet形式存在。富含甘氨酸和酪氨酸的多肽模块不仅存在于Suckerin嵌段多肽共聚物中,也在蜘蛛丝、蚕丝、贻贝足丝等嵌段多肽共聚物有广泛分布。该研究表明:富含甘氨酸和酪氨酸的多肽模块除了起到连接、间隔的作用之外,还能通过“微相分离”形成“分子胶”驱动嵌段多肽共聚物的自组装;Suckerin嵌段多肽共聚物的自组装分子机理的揭示,也有助于推动Suckerin嵌段多肽共聚物的广泛应用和新型仿生多肽纳米智能材料设计。
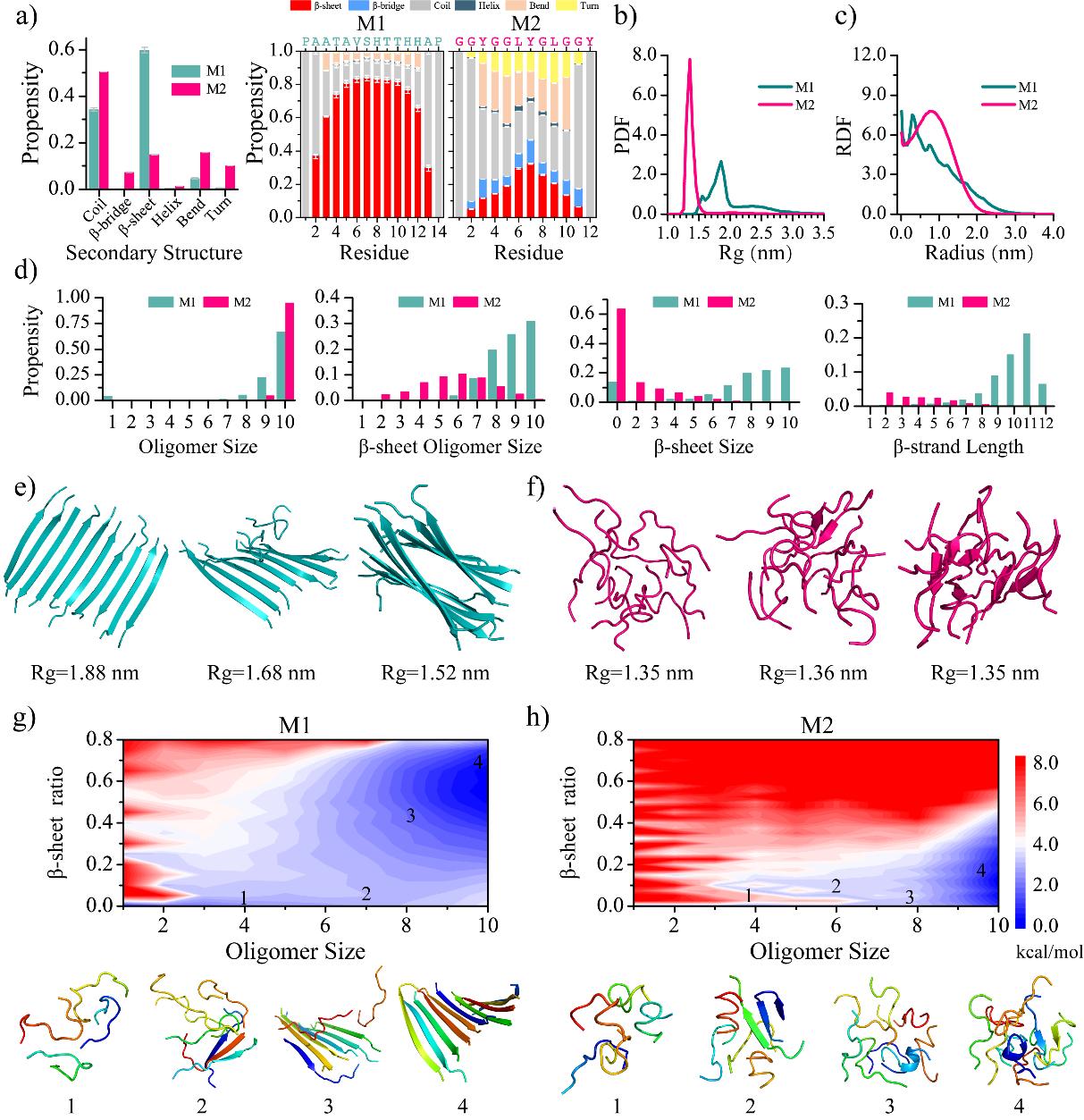
图1. M1、M2模块在275K的组装体构象分析。M1自组装分子结构呈现出高度有序延展β-sheet结构,M2则受疏水相互作用驱使塌缩成紧凑无序结构。
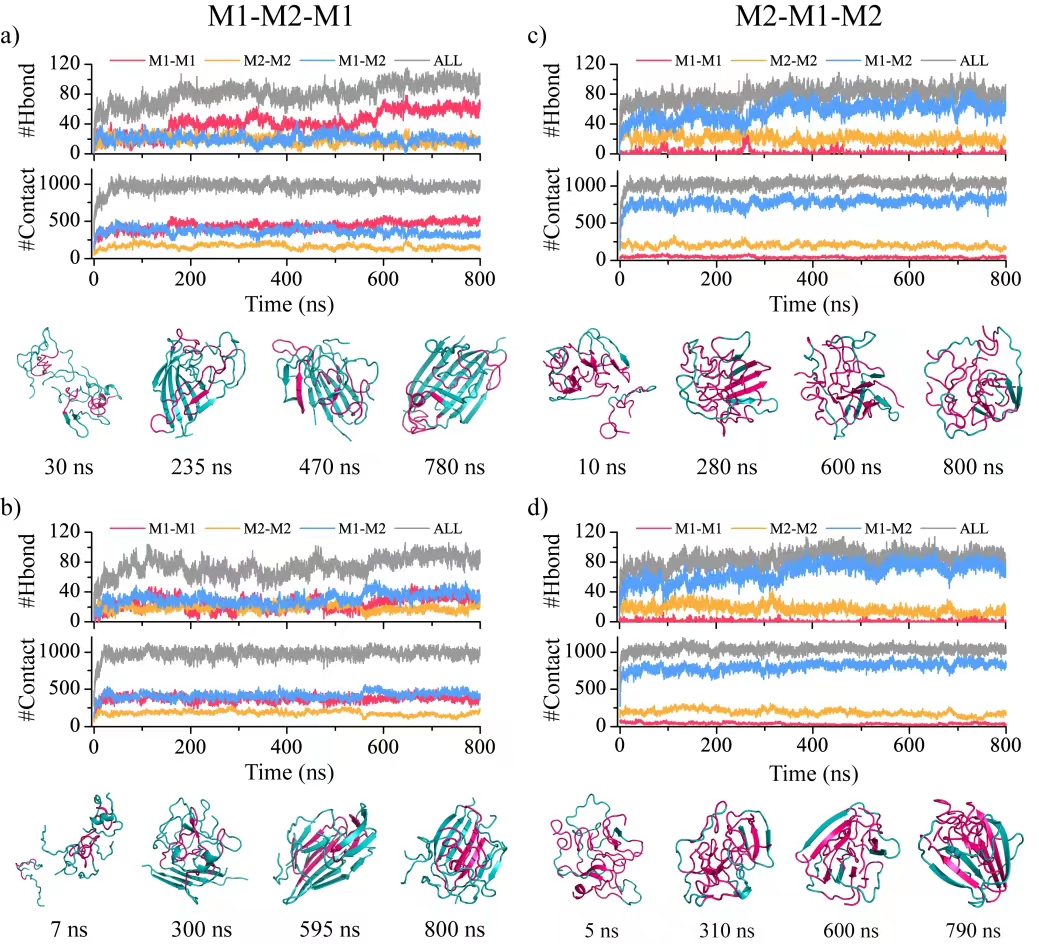
图2. 在M1-M2-M1和M2-M1-M2嵌段共聚物在275K自组装动力学过程。M1和M2模块聚集能力的差异性使得M1-M2-M1和M2-M1-M2嵌段多肽共聚物自组装成“微相分离”复合结构体。M2模块塌缩成柔软的“分子胶”,M1模块以β-sheet结构形式被粘附在M2“分子胶”周围。
论文链接:https://onlinelibrary.wiley.com/doi/full/10.1002/smll.202202642

